21世紀(jì)經(jīng)濟(jì)報(bào)道記者 季媛媛 上海報(bào)道 1月20日,日內(nèi)瓦藥品專利池組織(Medicines Patent Pool, MPP)宣布,已與包括復(fù)星醫(yī)藥(600196)、博瑞醫(yī)藥(688166)、迪賽諾醫(yī)藥、朗華制藥、龍澤制藥在內(nèi)的全球27家企業(yè)簽訂協(xié)議,將為全球105個(gè)中低收入國家或地區(qū)生產(chǎn)及供應(yīng)高質(zhì)量、可負(fù)擔(dān)的默沙東口服抗新冠病毒藥物Molnupiravir仿制藥。
受此消息影響,今日(1月21日)A股開盤,復(fù)星醫(yī)藥、博瑞醫(yī)藥皆漲停。
1月21日中午,博瑞醫(yī)藥發(fā)布公告稱,根據(jù)協(xié)議,除了專利許可使用費(fèi),產(chǎn)品授權(quán)各方不享受產(chǎn)品銷售分成,根據(jù)購買方性質(zhì)的不同,公司應(yīng)按照該產(chǎn)品年度凈銷售額(定義依據(jù)協(xié)議)的5%或10%向默沙東支付專利許可使用費(fèi),但基于MSD-MPP協(xié)議,前述專利許可使用費(fèi)將自WHO宣布COVID-19不再被列為“國際關(guān)注的突發(fā)公共衛(wèi)生事件”的次月起開始收取。
此外,本次許可項(xiàng)下合作藥品的生產(chǎn)前,尚需完成相關(guān)技術(shù)交接;生產(chǎn)設(shè)施需經(jīng)SRA(嚴(yán)格監(jiān)管機(jī)構(gòu),包括國際人類用藥技術(shù)要求協(xié)調(diào)理事會(ICH)成員、或ICH觀察員及與ICH成員相關(guān)監(jiān)管機(jī)構(gòu)等)批準(zhǔn)或經(jīng)世界衛(wèi)生組織預(yù)審合格。本次許可項(xiàng)下合作藥品在區(qū)域內(nèi)的生產(chǎn)、銷售等,須待相關(guān)主管機(jī)構(gòu)批準(zhǔn)(包括但不限于上市批準(zhǔn))后方可實(shí)施。公司于本次許可下生產(chǎn)的合作藥品在區(qū)域內(nèi)能否獲得當(dāng)?shù)厮幤繁O(jiān)管機(jī)構(gòu)上市批準(zhǔn)、于區(qū)域內(nèi)的上市時(shí)間存在不確定性。
當(dāng)前新冠病毒仍在全球大流行,新變種奧密克戎已經(jīng)在全球150多個(gè)國家和地區(qū)傳播,并且在多國已成為主要流行株。其中,中國已經(jīng)有14個(gè)省份報(bào)告奧密克戎輸入病例,而天津、河南、深圳等地還出現(xiàn)了本土奧密克戎疫情。
新冠口服特效藥被認(rèn)為是有望成為終結(jié)疫情的最后一張“拼圖”,此次雖然有5家中國企業(yè)獲得仿制許可,但是作為全球最大的發(fā)展中國家,這些企業(yè)生產(chǎn)的默沙東新冠口服藥仿制藥將不會在中國市場上市銷售,為什么中國不在受惠國名單之列?
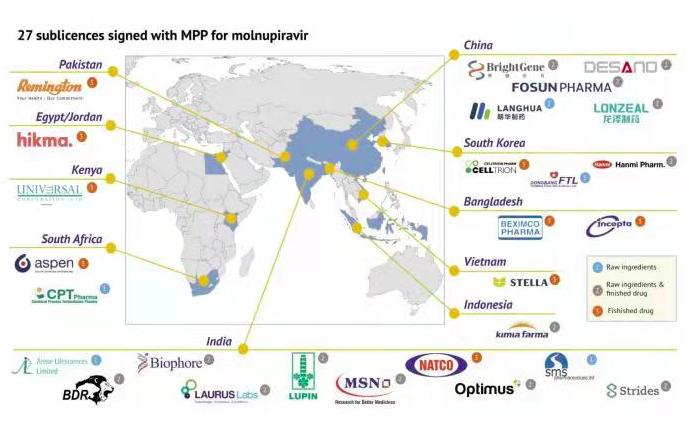
此次仿制藥為何不能在中國市場銷售?
21世紀(jì)經(jīng)濟(jì)報(bào)道記者通過查詢相關(guān)論文資料獲知,藥品專利池(MedicinesPatent Pool, MPP)是2010年在瑞士日內(nèi)瓦成立的。MPP通過與原研藥企就藥品專利的自愿許可進(jìn)行談判,原研藥企將其藥品專利放入專利池中,仿制藥企向MPP申請獲得專利池中的專利實(shí)施許可,生產(chǎn)并向中低收入國家供應(yīng)仿制藥。
仿制藥企(主要面向發(fā)展中國家制藥企業(yè))一是自愿將其相關(guān)藥品專利納入MPP;二是自愿向MPP提交被許可意向,被許可意向經(jīng)MPP專家評議通過后,MPP與仿制藥公司簽署許可協(xié)議,向原研公司給付許可費(fèi)并向MPP支付中介費(fèi)。獲得再許可的仿制藥企可被允許在發(fā)展中國家生產(chǎn)原研公司的專利藥品, 并依照許可協(xié)議規(guī)定,將所生產(chǎn)的專利藥品銷往低等和中低等收入國家。MPP許可為非獨(dú)占許可,并常通過許可多家仿制藥企業(yè)來增加市場競爭,降低藥品價(jià)格。概而言之,MPP平衡了原研公司與仿制藥商之間的利益,且有效解決了患者的藥物可及性問題及其與生命健康權(quán)之間的沖突問題。
此外,MPP許可有市場限制。再許可主要面向131個(gè)低等和中低等收入國家,但不包括中國、歐美等重要市場,意在將原研公司“放棄”的市場分享給仿制藥企。且不同藥品銷往的國家和地區(qū)有所不同。像巴西和中國這樣的大市場通常不被列入許可銷售的地理范圍內(nèi)。比如,從MPP網(wǎng)站公開的信息顯示,此前有三家中國藥企獲得了關(guān)于富馬酸替諾福韋二吡呋酯(TDF)的MPP許可,根據(jù)許可協(xié)議,中國藥企生產(chǎn)的TDF仿制藥(包括含有TDF組合制劑)可以銷往112個(gè)國家,但中國不在其列。2017年9月,吉利德與MPP修改了關(guān)于替諾福韋艾拉酚胺(TAF)的許可協(xié)議。與原來的協(xié)議相比,許可銷售國家范圍擴(kuò)大至116個(gè)國家。但有36個(gè)中等收入國家被排除在許可協(xié)議的地理范圍外。
現(xiàn)有的MPP許可覆蓋共達(dá)131個(gè)國家,涵蓋世界銀行標(biāo)準(zhǔn)下所有低收入國家和50%-80%的中等收入國家。
按世界銀行2021年7月發(fā)布的最新標(biāo)準(zhǔn),高收入國家為人均GNI(國民總收入)超過12695美元;中等偏上收入國家人均GNI超過4096美元,但低于12695美元;中等偏低收入國家人均GNI在1046美元到4096美元之間;人均GNI低于1046美元的,均屬于低收入國家。根據(jù)2021年中國經(jīng)濟(jì)年報(bào),2021年我國人均GDP達(dá)到80976元,按年平均匯率折算,已突破1.2萬美元,而GDP與GNI差距很小,如此對照中國應(yīng)在中等偏上國家之列。
中國患者何時(shí)能用上新冠口服藥?
默沙東方面表示,截至2021年底已生產(chǎn)了1000萬療程,預(yù)計(jì)2022年將至少生產(chǎn)2000萬療程。截至目前,默沙東已經(jīng)向獲得上市批準(zhǔn)或使用授權(quán)的20多個(gè)國家/地區(qū)運(yùn)送Molnupiravir,已經(jīng)有患者開始接受該藥物進(jìn)行治療。為了增加已獲許可的仿制藥制造商的供應(yīng)量,默沙東已經(jīng)與聯(lián)合國兒童基金會達(dá)成一項(xiàng)協(xié)議,在2022年上半年向中低收入國家/地區(qū)調(diào)配總計(jì)300萬療程Molnupiravir。
但事實(shí)上,新冠口服治療藥物供應(yīng)量遠(yuǎn)不能滿足需求量。據(jù)悉,輝瑞的Paxlovid需要6到8個(gè)月的生產(chǎn)時(shí)間。輝瑞與美國政府簽訂協(xié)議中的首批1000萬劑療程需到6月才能交付。默沙東表示,1月底將能交付300萬劑療程的Molnupiravir;,但因默沙東的藥物療效較低,需求有所減少。
據(jù)中泰證券報(bào)告,美國衛(wèi)生與公眾服務(wù)部數(shù)據(jù)顯示,自2021年9月以來,全美截至目前共分發(fā)抗新冠病毒藥物近300萬,包括257萬劑抗體注射藥物及36萬療程口服藥物。其中,默沙東口服藥則占總分發(fā)口服藥數(shù)量83%,合計(jì)分發(fā)30萬療程,但近期全美新增確診日均150萬例左右,遠(yuǎn)遠(yuǎn)供不應(yīng)求。
此外,有消息人士對21世紀(jì)經(jīng)濟(jì)報(bào)道記者透露,預(yù)計(jì)輝瑞將在2月初公布授權(quán)合作的企業(yè),為全球中低收入國家或地區(qū)生產(chǎn)及供應(yīng)高質(zhì)量、可負(fù)擔(dān)的口服抗新冠病毒藥物Paxlovid仿制藥。
此前輝瑞已與聯(lián)合國支持的非營利組織MMP達(dá)成了自愿許可協(xié)議。獲得MPP授權(quán)的合格仿制藥生產(chǎn)商將能夠向95個(gè)中低收入國家以更低的價(jià)格提供該藥。
國盛證券也分析,當(dāng)前企業(yè)申請輝瑞的MPP許可應(yīng)該也都已經(jīng)遞交了。根據(jù)科倫藥業(yè)平臺上回復(fù)投資者的問答,科倫遞交了申請,其他企業(yè)遞交的情況暫時(shí)無法確定。在此之前,雅本化學(xué)因“向輝瑞供應(yīng)卡龍酸酐”的傳聞而持續(xù)大漲,但后被公司否認(rèn),目前公司仍在停牌當(dāng)中。金城藥業(yè)也因中間體一度大漲。
至于此次錯(cuò)過了默沙東Molnupiravir仿制藥許可機(jī)會的企業(yè),還有誰能拿下輝瑞的Paxlovid仿制藥授權(quán)。
雖然MPP許可生產(chǎn)的默沙東及后續(xù)的輝瑞新冠口服藥仿制藥無法在中國市場銷售,但是對中國患者影響不大。對此有證券分析人士對21世紀(jì)經(jīng)濟(jì)報(bào)道記者指出,一是中國疫情控制得比較好,患者數(shù)量少需求本身就少;二是國產(chǎn)新冠口服藥進(jìn)展也很快,預(yù)計(jì)今年可提交上市申請。
此前,國產(chǎn)新冠口服藥VV116已在烏茲別克斯坦獲緊急使用授權(quán)。有市場消息認(rèn)為,在通過臨床試驗(yàn)后,君實(shí)生物有望在2022年下半年申請VV116上市。對此,君實(shí)生物在接受21世紀(jì)經(jīng)濟(jì)報(bào)道記者采訪時(shí)表示,公司目前正在積極推進(jìn)VV116的臨床試驗(yàn),正在準(zhǔn)備該藥物國際多中心二、三期臨床試驗(yàn)。
除了君實(shí)生物,國產(chǎn)在研新冠口服藥還包括開拓藥業(yè)AR拮抗劑普克魯胺目前處于全球三期臨床中,此前已在巴拉圭獲批EUA;真實(shí)生物阿茲夫定目前正在中國、巴西、俄羅斯開展III期臨床試驗(yàn),初步數(shù)據(jù)良好;前沿生物美國I期臨床正在進(jìn)行;先聲藥業(yè)針對SARS-CoV-2 病毒復(fù)制必須的關(guān)鍵蛋白酶3CL,在臨床前動(dòng)物模型上顯示了良好的抗病毒活性和安全性;云頂新耀宣布與新加坡公共研發(fā)機(jī)構(gòu)達(dá)成合作協(xié)議,引進(jìn)其新冠口服藥EDDC-2214。
MPP供應(yīng)協(xié)議將對哪些企業(yè)產(chǎn)生利好?
這個(gè)供應(yīng)協(xié)議,除了復(fù)星醫(yī)藥,也讓博瑞醫(yī)藥成為了一大贏家。
博瑞醫(yī)藥2021三季報(bào)顯示,公司主營收入7.48億元,同比上升46.62%;凈利潤1.77億元,同比上升45.3%。而在1月初,博瑞醫(yī)藥披露公告,公司擬以1000萬元認(rèn)購江蘇保易制藥有限公司人民幣116.67萬元的新增注冊資本。增資完成后,公司直接持有保易制藥3.92%股權(quán),保易制藥不納入公司合并報(bào)表范圍。博瑞醫(yī)藥擬與保易制藥在訂單生產(chǎn)及產(chǎn)品研發(fā)方面展開合作,以整體提升公司制藥技術(shù)綜合能力,完善“起始物料→高難度中間體-→特色原料藥→制劑”的全產(chǎn)業(yè)鏈布局。
此外,博瑞醫(yī)藥披露,公司在產(chǎn)能方面,截至2021年三季度末,泰興基地進(jìn)度為81.5%、蘇州項(xiàng)目已完成樁基和支護(hù)工程,印尼項(xiàng)目土建完成率95%。
據(jù)民生證券指出,輝瑞Paxlovid國內(nèi)合作供應(yīng)商為博騰股份、凱萊英等;默沙東Molnupiravir國內(nèi)合作供應(yīng)商為天宇股份、博騰股份等,美國政府已經(jīng)訂購了1000萬療程輝瑞藥物和300萬療程默沙東藥物,預(yù)計(jì)全球訂單量將進(jìn)一步增長。
某醫(yī)藥行業(yè)首席分析師對21世紀(jì)經(jīng)濟(jì)報(bào)道記者表示,也是受到此次MMP協(xié)議的推動(dòng),原料藥、CDMO供應(yīng)商也會迎來了多番利好。在五家本土藥企獲默沙東口服藥仿制許可,為全球105個(gè)中低收入國家或地區(qū)生產(chǎn)及供應(yīng)新冠口服藥Molnupiravir仿制藥后,這意味著,后續(xù)原料藥、CDMO供應(yīng)商將繼續(xù)放量。
此前,中國醫(yī)藥保健品進(jìn)出口商會分會秘書長朱仁宗在接受21世紀(jì)經(jīng)濟(jì)報(bào)道記者采訪時(shí)表示,從2020年吉利德“瑞德西韋”開始,中國原料藥、CXO企業(yè)或多或少已經(jīng)加入到新冠肺炎治療藥物研發(fā)鏈條中,承接新冠肺炎相關(guān)治療藥物的原料藥、中間體服務(wù)單。除了在藥物研發(fā)階段,這些企業(yè)還會得到代加工訂單,接下來,在新冠肺炎治療藥物走向獲批上市階段后,也將會實(shí)現(xiàn)巨大的商業(yè)附加利益,畢竟全球新冠肺炎患者數(shù)量較為龐大。
而安永大中華區(qū)生命科學(xué)與醫(yī)療健康行業(yè)聯(lián)席主管合伙人吳曉穎此前在接受21世紀(jì)經(jīng)濟(jì)報(bào)道記者采訪時(shí)也指出,在新冠全球大流行的背景下,市場寄希望于新冠疫苗+新冠病毒治療藥物的組合可以使得新冠 “流感化”。 如此也會使得短期內(nèi)由于中國原料藥在全球供應(yīng)鏈中的地位以及良好的國內(nèi)疫情管控,部分和跨國藥企深度合作的原料藥生產(chǎn)廠商已經(jīng)收獲第一波業(yè)務(wù)機(jī)會,而長遠(yuǎn)看,隨著市場趨于常態(tài),越來越多的小分子藥物上市使得價(jià)格回歸合理區(qū)間,假設(shè)新冠口服小分子市場在百億美金規(guī)模,5%-6%原料藥市場,帶來新的市場空間約為每年5-6億美金。


















 粵公網(wǎng)安備 44010402000579號
粵公網(wǎng)安備 44010402000579號