這里是《21健訊Daily》,歡迎與21世紀經濟報道新健康團隊共同關注醫藥健康行業最新事件!
一、政策動向
●國家藥監局:6家化妝品生產企業飛檢違規
9月8日,國家藥監局發布關于廣州總都國際生物科技有限公司等企業飛行檢查結果的通告(2023年第44號)。
近期,國家藥監局組織對廣州總都國際生物科技有限公司、億通生物科技(廣州)有限公司、汕頭市玉潔化妝品有限公司、廣州市秀語化妝品有限公司、廣州市妝妍生物技術有限公司、廣州赫蘭迪生物科技有限公司6家化妝品生產企業進行了飛行檢查。經查,發現上述企業違反了《化妝品監督管理條例》《化妝品生產質量管理規范》等有關規定。上述企業已對存在的問題予以確認。為保障公眾用妝安全,國家藥監局要求廣東省藥品監督管理局對企業上述涉嫌違法行為依法予以處理。廣東省藥品監督管理局目前已責令上述企業暫停生產、經營并進行整改,同時對其立案調查。
●第五批“港澳藥械通”目錄發布
9月8日,根據《粵港澳大灣區藥品醫療器械監管創新發展工作方案》(國市監藥〔2020〕159號)和《廣東省粵港澳大灣區內地臨床急需進口港澳藥品醫療器械管理暫行規定》(粵藥監規許〔2021〕4號)要求,結合工作實際,廣東省藥品監督管理局、廣東省衛生健康委員會發布第五批粵港澳大灣區內地臨床急需進口港澳藥品醫療器械目錄。

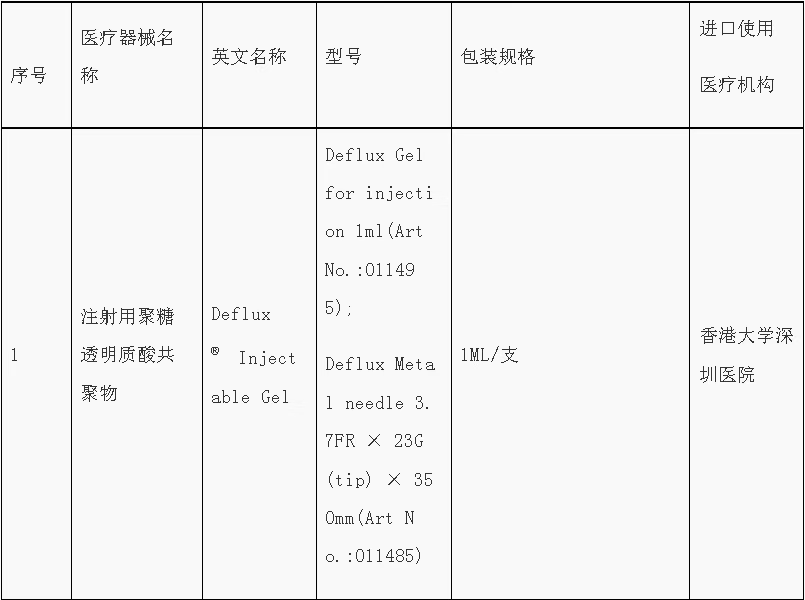
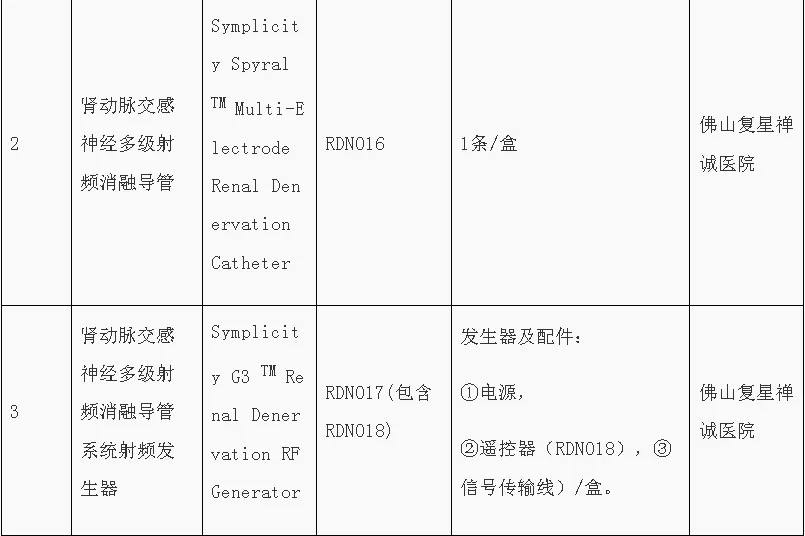


●《關于支持在橫琴粵澳深度合作區使用澳門地區已上市部分藥品的工作方案》發布
9月8日,廣東省藥品監督管理局、廣東省發展和改革委員會、廣東省衛生健康委員會、中華人民共和國海關總署廣東分署聯合發布關于印發《關于支持在橫琴粵澳深度合作區使用澳門地區已上市部分藥品的工作方案》的通知。
方案指出,按照《中華人民共和國藥品管理法》《橫琴粵澳深度合作區建設總體方案》《粵港澳大灣區藥品醫療器械監管創新發展工作方案》《廣東省粵港澳大灣區內地臨床急需進口港澳藥品醫療器械管理暫行規定》等有關規定,在合作區內允許澳門居民使用澳門地區已上市部分藥品,進一步推動粵澳兩地醫療和用藥等民生公共服務銜接,有效拓展澳門居民優質生活空間。
一是適用范圍。關于醫療機構范圍:適用于合作區內為澳門居民提供基礎醫療服務的指定醫療機構。關于使用藥品品種范圍:適用于除生物制品外的已在澳門地區上市的部分藥品(以下簡稱指定澳門藥品,指定澳門藥品不含實施進出口準許證管理的麻醉藥品、精神藥品、興奮劑目錄中的蛋白同化制劑和肽類激素、藥品類易制毒化學品、放射性藥品等品種)。指定澳門藥品實行目錄管理,藥品目錄由廣東省藥品監督管理局(以下簡稱省藥監局)、廣東省衛生健康委員會(以下簡稱省衛生健康委)會同澳門藥品監管部門審核確定并動態調整。
二是相關要求及流程。省衛生健康委根據指定醫療機構申請或者合作區衛生健康部門推薦,負責審核為澳門居民提供基礎醫療服務的指定醫療機構。
合作區內指定醫療機構向省藥監局提出指定澳門藥品申請,并提交經澳門藥品監管部門審核確定后的用藥清單,經廣東省藥監局和廣東省衛生健康委批準后,可以在合作區內指定醫療機構中提供給澳門居民使用。
三是監督管理。廣東省藥監局按照粵澳雙方簽訂的《粵港澳大灣區藥品醫療器械監管協作備忘錄》,加強與澳門特別行政區政府藥品監管部門合作,指導合作區藥品監督管理部門開展監管工作。合作區衛生健康部門依法對指定醫療機構的診療行為進行日常監管。合作區藥品監督管理部門依法對指定澳門藥品在合作區內運輸、貯存、經營等過程進行日常監管。同時,加強與澳門特別行政區政府藥品監督管理部門銜接,通過建立合作機制、簽訂備忘錄等方式,實現藥品安全信息互通共享,制定應急處置協作機制,加強對指定澳門藥品的全生命周期安全管理。
二、藥械審批
●百拓維?(戈舍瑞林微球)在中國獲批乳腺癌適應癥
9月7日,百濟神州與綠葉制藥集團宣布,綠葉制藥自主研發的創新制劑注射用戈舍瑞林微球(中文商標:百拓維?)已獲得中國國家藥品監督管理局(NMPA)批準,用于可用激素治療的絕經前期及圍絕經期婦女的乳腺癌患者。
自今年6月30日百拓維?在中國獲批用于前列腺癌的治療以來,百濟神州便與綠葉制藥攜手,快速開啟該產品惠及患者的整體進程,第一時間投入臨床使用。此次新適應癥的獲批,意味著百拓維?覆蓋的患者群體將進一步擴大。
●抗癌新藥“米托坦片”在中國獲批上市
9月8日,中國國家藥品監督管理局(NMPA)官網最新公示,HRA Pharma Rare Diseases公司的米托坦片(mitotane)已在中國獲批上市。根據優先審評公示信息,該藥本次獲批的適應癥為腎上腺皮質癌(ACC)。
米托坦是一種腎上腺細胞毒性活性物質,可抑制腎上腺皮質產生皮質類固醇激素。對米托坦作用方式的研究發現,該藥有兩個主要的生物學效應:一是通過線粒體改變和抑制甾醇-O-酰基轉移酶1(SOAT1)的活性,米托坦可對腎上腺皮質細胞產生直接的細胞毒性作用;二是通過改變皮質醇的外周代謝并直接抑制腎上腺皮質分泌皮質類固醇,來抑制皮質類固醇的合成。
●蓉生藥業重組凝血因子Ⅷ正式獲批
9月8日,中國國家藥品監督管理局(NMPA)官網最新公示,由天壇生物子公司蓉生藥業申請的注射用重組凝血因子Ⅷ已正式獲批。公開資料顯示,該產品擬開發用于治療血友病A患者。
公開資料顯示,血友病A是一種由凝血因子Ⅷ(Coagulation Factor Ⅷ,FⅧ)缺乏而導致的出血性疾病,是X染色體連鎖的隱性遺傳性疾病,主要由凝血因子Ⅷ基因突變引起。若反復出血不及時治療,可導致關節畸形和(或)假腫瘤形成,嚴重者可危及生命。
三、資本市場
●沙礫生物完成4億元B輪融資
9月8日,沙礫生物(Grit Biotechnology)宣布完成4億元 的B輪融資,本輪融資由中金資本旗下基金領投,前海方舟、聯東投資、源禾資本、禾方田合伙企業以及原股東夏爾巴投資、德誠資本、經緯中國跟投。
本輪融資將用于支持其腫瘤浸潤淋巴細胞(TIL)療法管線的開發,包括GT101的關鍵臨床試驗以及多項下一代基因編輯型TIL管線的開發,致力于為全球實體瘤患者打造開創性細胞藥物。
四、行業大事
●北京首次“DGR+集采”聯動中選結果公布
近日,北京市醫保局官網公布了該市《第一批DRG付費和帶量采購聯動 管理采購產品中選結果》。
北京市DRG付費和帶量采購聯動,由安貞醫院、積水潭醫院、天壇醫院、阜外醫院、北醫三院、宣武醫院等6家三甲醫院組成的DRG聯動采購集團牽頭,聯合北京市公立醫療機構組建聯盟,針對運動醫學類、神經介入類、電生理類醫用耗材,制定了DRG付費和帶量采購聯動管理方案。其中,1號公告針對神經介入類彈簧圈產品(包括但不限于以國家醫保耗材編碼C020516065前10位開頭),采取帶量聯動方式;2號公告針對上市運動醫學類、神經介入類、電生理類醫用耗材產品采取帶量談判方式,其中“顱內支架-覆膜支架”只進行價格談判不帶量。盡管采購方式不同,但全市醫保定點醫療機構均可作為采購主體參加本次DRG聯動采購。采取帶量談判的產品,按照國家醫保醫用耗材分類與代碼前10位分別確定電生理、運動醫學、神經介入三類醫用耗材采購產品。

















